AG Schlaf
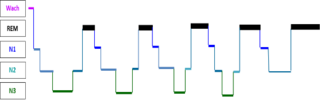
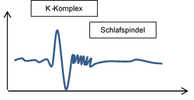
Die Arbeitsgruppe Schlafstörungen befasst sich mit der klinischen Forschung bei neurologischen Schlafstörungen. Unser Schwerpunkt liegt dabei insbesondere auf der Untersuchung der REM-Schlafverhaltensstörung sowie von Schlafstörungen bei neurodegenerativen Erkrankungen wie dem idiopathischen Parkinsonsyndrom, Demenzen und Motoneuronerkrankungen. Hintergrund ist, dass Patienten mit neurodegenerativen Erkrankungen wie dem idiopathischen Parkinsonsyndrom meist vor allem in Hinblick auf ihre motorischen und / oder kognitiven Probleme behandelt werden, wohingegen die nicht-motorischen Störungen, wie Schlafstörungen im Alltag oft weniger stark berücksichtig werden, obwohl sie sehr häufig sind und die Patienten stark belasten. Die Mechanismen, die zu Schlafstörungen führen, sind bei diesen Patienten noch nicht vollständig verstanden. Unsere Forschung zielt somit auf die Untersuchung und das bessere Verständnis von Schlafstörungen und deren Bedeutung sowie mögliche Behandlungsoptionen für die Patienten ab.
Einzelprojekte
Verbesserung des Verständnis und der Auswirkungen von Schlafstörungen bei neurodegenerativen Erkrankungen
Zum besseren Verständnis von Schlafstörungen bei neurodegenerativen Erkrankungen führen wir detaillierte Untersuchungen des Schlafs bei diesen Patienten mit verschiedenen Techniken (vor allem Polysomnographie, Aktigraphie) durch. Zudem wollen wir Mechanismen der Ursachen von Schlafstörungen sowie den bidirektionalen Zusammenhang zwischen Schlaf und Neurodegeneration beleuchten. Hierzu wollen wir u.a. die Wirkungsweise des sogenannten glymphatischen Systems, das eine wichtige Rolle bei der Elimination neurotoxischer Stoffe im Gehirn zu spielen scheint, untersuchen. Zudem sollen die Auswirkungen von Schlafstörungen bei Patienten mit neurodegenerativen Erkrankungen auf das Befinden (u.a. Depression, autonome Störungen) und die Kognition untersucht werden. Wir beschäftigen uns zudem mit der Frage, wie sich Schlafstörungen, z.B. bei Motoneuronerkrankungen, auf das Befinden und das Überleben auswirken und welchen Einfluß die Beatmung bei diesen Patienten hat. Dies ist entscheidend, um die Wichtigkeit von Schlafstörungen für die Patienten deutlich zu machen und mögliche Therapieformen zu etablieren. Zukünftig ist geplant, den Patienten anhand dieser Ergebnisse auch gezielte Therapieoptionen anzubieten.
Früherkennung der Konversion zu neurodegenerativen Erkrankungen
Darüber hinaus scheint es Zusammenhänge zwischen Schlafstörungen und dem Auftreten neurodegenerativer Erkrankungen zu geben, deren Grundlagen noch nicht ausreichend verstanden sind. So entwickeln Patienten mit einer REM-Schlafverhaltensstörung im Verlauf häufig eine neurodegenerative Erkrankung. Deshalb ist es von besonderer Bedeutung, Marker für eine bevorstehende Entwicklung hin zu einer neurodegenerativen Erkrankung zu identifizieren, um diese sogenannte Konversion in der Zukunft evtl. verhindern zu können. Zu diesem Zweck arbeiten wir sowohl an der klinischen Charakterisierung unserer Patienten wie beispielsweise der Charakterisierung autonomer Funktionsstörungen sowie an der Entwicklung von Biomarkern, z.B. der Haut, im Blut sowie in der Bildgebung (cMRT, PET) und im EEG (Deep learning).
Intervention zur Vermeidung der Konversion / des Fortschreitens von neurodegenerativen Erkrankungen
Aufbauend auf Erkenntnissen zu Mechanismen und Auswirkungen von Schlafstörungen in der Frühphase sowie der klinischen Phase neurodegenerativer Erkrankungen wollen wir uns in Zukunft mit den Interventionsmöglichkeiten bei Schlafstörungen, um evtl. eine Konversion bzw. das Fortschreiten neurodegenerativer Erkrankungen verhindern oder verzögern zu können, intensiver befassen und hierzu neuartige Strategien anwenden.
Vereinfachung und Verbesserung der Diagnostik von Schlafstörungen
Unsere Projekte in diesem Bereich zielen auf die Vereinfachung der Diagnostik von Schlafstörungen durch Anwendung neuer technischer Applikationen wie z.B. Aktimetrie oder vereinfachtem Schlaf-EEG ab. Dies würde die Messung von Schlafstörungen über längere Zeiträume und in der für den Patienten gewohntem Umgebung vereinfachen und somit technische Limitationen der bisherigen Schlaflabor-Diagnostik umgehen.
Kooperationen
Wir arbeiten an diesen Projekten sowohl national (u.a. AG Prof. Dr. S. Teipel (DZNE), Fr. PD Dr. H. Benes (Schlaflabor SomniBene Schwerin), Dr. M. Brandt / Prof. Dr. T. Ziemssen (Neurologie / UKD Dresden), Deutsche RBD Studiengruppe als auch international (Internationale RBD Study Group) vernetzt zusammen.
Ausgewählte Publikationen:
- Hermann W, Flemming T, Brandt MD, Langner S, Reichmann H, Storch A. Asymmetry of Periodic Leg Movements in Sleep (PLMS) in Parkinson's Disease. J Parkinsons Dis. 2019 Oct 4. doi: 10.3233/JPD-191667
- Zhang R, Werner A, Hermann W, Brandt MD, Beste C, Stock AK. Thalamic GABA may modulate cognitive control in restless legs syndrome. Neurosci Lett. 2019 Nov 1;712:134494. doi: 10.1016/j.neulet.2019.134494. Epub 2019 Sep 11.
- Löhle M, Hermann W, Hausbrand D, Wolz M, Mende J, Beuthien-Baumann B, Oehme L, van den Hoff J, Kotzerke J, Reichmann H, Hermann A, Storch A. Putaminal Dopamine Turnover in de novo Parkinson's Disease Predicts Later Neuropsychiatric Fluctuations but Not Other Major Health Outcomes. J Parkinsons Dis. 2019;9(4):693-704. doi: 10.3233/JPD-191672
- Ritter P, Brandt M, Schrempf W, Brezan F, Krupka A, Storch A, Sauer C, Pfennig A, Bauer M, Soltmann B. Role of the IL-6-Receptor expression in CD14+ monocytes in modulating sleep in patients with bipolar disorder. J Affect Disord. 2018 Oct 15;239:152-160. doi: 10.1016/j.jad.2018.06.037.
- Ritter PS, Schwabedal J, Brandt M, Schrempf W, Brezan F, Krupka A, Sauer C, Pfennig A, Bauer M, Soltmann B, Nikitin E. Sleep spindles in bipolar disorder - a comparison to healthy control subjects. Acta Psychiatr Scand. 2018 Jul 4. doi: 10.1111/acps.12924.
- Schrempf W, Fauser M, Wienecke M, Brown S, Maaß A, Ossig C, Otto K, Brandt MD, Löhle M, Schwanebeck U, Graehlert X, Reichmann H, Storch A. Rasagiline improves polysomnographic sleep parameters in patients with Parkinson's disease: a double-blind, baseline-controlled trial. Eur J Neurol. 2018 Apr;25(4):672-679.
- Günther R, Schrempf W, Hähner A, Hummel T, Wolz M, Storch A, Hermann A. Impairment in Respiratory Function Contributes to Olfactory Impairment in Amyotrophic Lateral Sclerosis. Front Neurol. 2018 Feb 26;9:79.
- Zhang R, Schrempf W, Brandt MD, Mückschel M, Beste C, Stock AK. RLS patients show better nocturnal performance in the Simon task due to diminished visuo-motor priming. Clin Neurophysiol. 2018 Jan;129(1):112-121.
- Zhang R, Brandt MD, Schrempf W, Beste C, Stock AK. Neurophysiological mechanisms of circadian cognitive control in RLS patients - an EEG source localization study. Neuroimage Clin. 2017 Jun 15;15:644-652.
- Lahut S, Gispert S, Ömür Ö, Depboylu C, Seidel K, Domínguez-Bautista JA, Brehm N, Tireli H, Hackmann K, Pirkevi C, Leube B, Ries V, Reim K, Brose N, den Dunnen WF, Johnson M, Wolf Z, Schindewolf M, Schrempf W, Reetz K, Young P, Vadasz D, Frangakis AS, Schröck E, Steinmetz H, Jendrach M, Rüb U, Başak AN, Oertel W, Auburger G. Blood RNA biomarkers in prodromal PARK4 and REM sleep behavior disorder show role of complexin-1 loss for risk of Parkinson's disease. Dis Model Mech. 2017 Jan 20.
- Siepmann T, Frenz E, Penzlin AI, Goelz S, Zago W, Friehs I, Kubasch ML, Wienecke M, Löhle M, Schrempf W, Barlinn K, Siegert J, Storch A, Reichmann H, Illigens BM. Pilomotor function is impaired in patients with Parkinson's disease: A study of the adrenergic axon-reflex response and autonomic functions. Parkinsonism Relat Disord. 2016 Oct;31:129-134.
- Schrempf W*, Katona I*, Dogan I, Felbert VV, Wienecke M, Heller J, Maier A, Hermann A, Linse K, Brandt MD, Reichmann H, Schulz JB, Schiefer J, Oertel WH, Storch A, Weis J, Reetz K. Reduced intraepidermal nerve fiber density in patients with REM sleep behavior disorder. Parkinsonism Relat Disord. 2016 Aug;29:10-6. *These authors contributed equally.
- Kepplinger J, Barlinn K, Boehme AK, Gerber J, Puetz V, Pallesen LP, Schrempf W, Dzialowski I, Albright KC, Alexandrov AV, Reichmann H, von Kummer R, Bodechtel U. Association of sleep apnea with clinically silent microvascular brain tissue changes in acute cerebral ischemia. J Neurol. 2014 Feb;261(2):343-9.
- Kepplinger J, Barlinn K, Kolieskova S, Shahripour RB, Pallesen LP, Schrempf W, Graehlert X, Schwanebeck U, Sisson A, Zerna C, Puetz V, Reichmann H, Albright KC, Alexandrov AW, Vosko M, Mikulik R, Bodechtel U, Alexandrov AV. Reversal of the neurological deficit in acute stroke with the signal of efficacy trial of auto-BPAP to limit damage from suspected sleep apnea (Reverse-STEAL): study protocol for a randomized controlled trial. Trials. 2013 Aug 13;14:252.
- Kepplinger J, Barlinn K, Albright KC, Schrempf W, Boehme AK, Pallesen LP, Schwanebeck U, Graehlert X, Storch A, Reichmann H, Alexandrov AV, Bodechtel U. Early sleep apnea screening on a stroke unit is feasible in patients with acute cerebral ischemia. J Neurol. 2013 May;260(5):1343-50.
Reviews:
- Schrempf W., Reichmann H. Schlafstörungen beim idiopathischen Parkinsonsyndrom. CME-Artikel 2017, Info Neurologie und Psychiatrie, Review
- Schrempf W. Aktuelle Therapie der Narkolepsie – Pitolisant erweitert die Therapieoptionen. Psychopharmakotherapie 2016;23:184-8. Review.
- Schrempf W, Brandt MD, Storch A, Reichmann H. Sleep disorders in Parkinson's disease. J Parkinsons Dis. 2014;4(2):211-21. doi: 10.3233/JPD-130301. Review.
